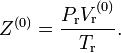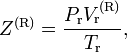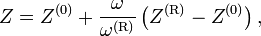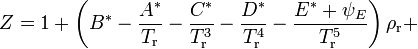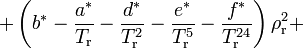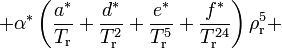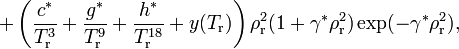- Уравнение состояния Бенедикта — Вебба — Рубина
-
Уравнение состояния Бенедикта — Вебба — Рубина
Уравнение состояния 
Статья является частью серии «Термодинамика». Уравнение состояния идеального газа Уравнение Ван-дер-Ваальса Уравнение Дитеричи Уравнение состояния Редлиха — Квонга Уравнение состояния Барнера — Адлера Уравнение состояния Суги — Лю Уравнение состояния Бенедикта — Вебба — Рубина Уравнение состояния Ли — Эрбара — Эдмистера Разделы термодинамики Начала термодинамики Уравнение состояния Термодинамические величины Термодинамические потенциалы Термодинамические циклы Фазовые переходы править Уравнение состояния Бенедикта — Вебба — Рубина (уравнение состояния Бенедикта — Уэбба — Рубина) — многопараметрическое уравнение состояния, полученное[1][2][3][4] в работах 1940—42 годов Мэнсоном Бенедиктом (Manson Benedict), Джорджем Веббом (Уэббом) (George B. Webb) и Льюисом Рубином (Louis C. Rubin) в ходе улучшения уравнения Битти — Бриджмена. Уравнение было получено корреляцией термодинамических и волюметрических данных жидких и парогазообразных лёгких углеводородов, а также их смесей. Уравнение, в отличие от уравнения Редлиха — Квонга, не является кубическим относительно коэффициента сжимаемости
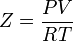 , однако при этом структура уравнения Бенедикта — Вебба — Рубина позволяет описывать состояние широкого класса веществ.
, однако при этом структура уравнения Бенедикта — Вебба — Рубина позволяет описывать состояние широкого класса веществ.Уравнение имеет вид:
где
- P — давление, Па;
- T — абсолютная температура, К;
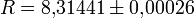 — универсальная газовая постоянная, Дж/(моль·К);
— универсальная газовая постоянная, Дж/(моль·К);- ρm — мольная плотность, моль/м³;
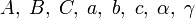 — восемь волюметрических констант конкретного вещества.
— восемь волюметрических констант конкретного вещества.
Имеется несколько наборов констант уравнения Бенедикта — Вебба — Рубина, которые различаются различными диапазонами применимости, например, в статье[5] Купера (H. W. Cooper) и Гольдфранка (J. C. Goldfrank) приведены константы для 33 веществ. Некоторые авторы[6] таблиц констант уравнения Бенедикта — Вебба — Рубина определяют их не из условия «наилучшего согласования» с P − V − T данными, а подбирают их так, чтобы улучшить обобщённую корреляцию констант для гомологических рядов. В связи с этим никогда не следует смешивать константы из различных таблиц. Все константы для данного вещества всегда должны быть взяты из одного источника.
Температурный диапазон применимости волюметрических констант почти всегда соответствует Tr > 0,6 (Tr = T / Tk — приведённая температура, Tk — критическая температура).
Содержание
Температурные модификации
В ходе обработки экспериментальных данных ряд авторов[7][8] стал отмечать, что при температурах ниже нормальной точки кипения коэффициент C уравнения Бенедикта — Вебба — Рубина лучше заменить на функцию температуры, для того чтобы уравнение более точно описывало давление паров.
Модификация Кауфмана
Кауфман (T. G. Kaufman) предложил[7] аппроксимацию вида:
где Ai — константы, зависящие от свойств вещества.
Модификация Орая
Наиболее тщательным количественный анализ проблемы зависимости C(T) был выполнен[9] Ораем (R. V. Orye). Он предложил следующую температурную зависимость для C:
- C1 / 2(T) = C1 / 2(T0) − ΔC1 / 2(T),
где C(T0) — значение константы C, а величина ΔC1 / 2(T) — является полиномом 5-ой степени.
- ΔC1 / 2(T) = Q1Θ2 + Q2Θ3 + Q3Θ4 + Q4Θ5,
где Θ = (T0 − T) / T0 — безразмерный комплекс температуры, T0 — реперная температура.
Модификация Старлинга
Старлинг (К. E. Starling) предложил[10][11] модифицировать уравнение Бенедикта — Вебба — Рубина таким образом, чтобы от температуры зависил не только коэффициент C, но и коэффициент a, получив тем самым уравнение состояния Бенедикта — Вебба — Рубина — Старлинга с одиннадцатью параметрами:
Область применимости —
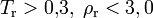 .
.Обобщённые модификации
Успешное использование оригинала уравнения Бенедикта — Вебба — Рубина при расчётах волюметрических и термодинамических свойств чистых газов и жидкостей обусловило появление ряда работ, в которых это уравнение или его модификация приводится к обобщённой форме, применимой ко многим типам соединений[12][13].
Модификация Ли — Кеслера
Ли (B. I. Lee) и Кеслер (M. G. Kesler) разработали[14] модифицированное уравнение состояния Бенедикта — Вебба — Рубина, используя трёхпараметрическую корреляцию Питцера[15]. По их методу коэффициент сжимаемости реального вещества связывается со свойствами простого вещества, для которого ω = 0, и н-октана, выбранного в качестве эталона. Для того чтобы рассчитать коэффициент сжимаемости вещества при некоторых значениях температуры и давления, используя критические свойства этого вещества, сначала следует определить приведённые параметры Tr и Pr. Затем рассчитывает идеальный приведённый объём простого вещества по уравнению:
где
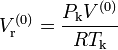 — идеальный приведённый объём простого вещества;
— идеальный приведённый объём простого вещества;- V(0) — мольный объём простого вещества, м³/моль;
- Pr = P / Pk — приведённое давление;
- Pk — критическое давление, Па;
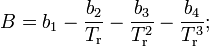
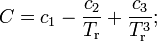
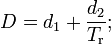
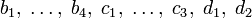 — коэффициенты.
— коэффициенты.
После определения V(0), рассчитывается коэффициент сжимаемости простого вещества:
Далее, используя те же приведённые параметры, определённые ранее, снова решается уравнение (*) относительно
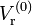 , но уже с константами для эталонного вещества. После этого находят коэффициент сжимаемости эталонного (опорного) вещества:
, но уже с константами для эталонного вещества. После этого находят коэффициент сжимаемости эталонного (опорного) вещества:где Z(R) — коэффициент сжимаемости эталонного вещества;
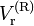 — приведённый объём эталонного вещества.
— приведённый объём эталонного вещества.Коэффициент сжимаемости Z интересующего вещества определяется из уравнения:
где
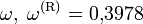 — фактор ацентричности (англ.) Питцера исследуемого и эталонного вещества (октана) соответственно.
— фактор ацентричности (англ.) Питцера исследуемого и эталонного вещества (октана) соответственно.Уравнение применяется в основном для углеводородов в интервалах значений
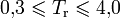 и
и 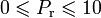 для паровой и жидкой фазы, где средняя погрешность составляет менее 2 %.
для паровой и жидкой фазы, где средняя погрешность составляет менее 2 %.Модификация Нишиуми
По утверждению[16] Хопке (S. W. Hopke), как уравнение Бенедикта — Вебба — Рубина, так и уравнение Бенедикта — Вебба — Рубина — Старлинга не дают возможность получить достаточно точные параметры для большинства полярных жидкостей и воды в частности.
Чтобы устранить этот недостаток Нишиуми (H. Hishiumi) разработал[17][18] обобщающую модификацию уравнения Бенедикта — Вебба — Рубина и привёл данные для 92-х веществ, в том числе воды.
Уравнение Нишиуми для коэффициента сжимаемости Z имеет вид:
где ρr = ρ / ρk — приведённая плотность, ρk — критическая плотность. Все пятнадцать коэффициентов, отмеченные «звездочками», являются функциями коэффициента ацентричности ω; величины ψE и y(Tr) выражают воздействие полярности на свойства паров и жидкостей соответственно.
Область применимости — Tr < 1,3 и 1 < Pr < 3.
Литература
- Рид Р., Праусниц Дж., Шервуд Т. Свойства газов и жидкостей: Справочное пособие / Пер. с англ. под ред. Б. И. Соколова. — 3-е изд. — Л.: Химия, 1982. — 592 с.
- Уэйлес С. Фазовые равновесия в химической технологии: В 2-х ч. Ч. 1. — М.: Мир, 1989. — 304 с. — ISBN 5-03-001106-4.
См. также
- Уравнение состояния идеального газа
- Уравнение Ван-дер-Ваальса
- Уравнение Дитеричи
- Уравнение состояния Редлиха — Квонга
- Уравнение состояния Барнера — Адлера
- Уравнение состояния Суги — Лю
- Уравнение состояния Ли — Эрбара — Эдмистера
Примечания
- ↑ Benedict M., Webb G. B., Rubin L. C. An Empirical Equation for Thermodynamic Properties of Light Hydrocarbons and Their Mixtures: I. Methane, Ethane, Propane, and n-Butane // Journal of Chemical Physics. — 1940. — В. 4. — Т. 8. — С. 334—345.
- ↑ Benedict M., Webb G. B., Rubin L. C. An Empirical Equation for Thermodynamic Properties of Light Hydrocarbons and Their Mixtures: II. Mixtures of Methane, Ethane, Propane and n-Butane // Journal of Chemical Physics. — 1942. — В. 12. — Т. 10. — С. 747—758.
- ↑ Benedict M., Webb G. B., Rubin L. C. An Empirical Equation for Thermodynamic Properties of Light Hydrocarbons and Their Mixtures: III. Constants for Twelve Hydrocarbons // Chemical Engineering Progress. — 1951. — В. 8. — Т. 47. — С. 419—422.
- ↑ Benedict M., Webb G. B., Rubin L. C. An Empirical Equation for Thermodynamic Properties of Light Hydrocarbons and Their Mixtures: IV. Fugacities and Liquid-Vapor Equilibria // Chemical Engineering Progress. — 1951. — В. 9. — Т. 47. — С. 449—454.
- ↑ Cooper H. W., Goldfrank J. C. // Hydrocarbon Processing. — 1967. — В. 12. — Т. 46. — С. 141.
- ↑ Bishnoi P. R., Miranda R. D., Robinson D. B. // Hydrocarbon Processing. — 1974. — В. 11. — Т. 53. — С. 197.
- ↑ 1 2 Kaufman T. G. Method for Phase Equilibrium Calculations Based on Generalized Benedict — Webb — Rubin Constants // Industrial and Engineering Chemistry Fundamentals. — 1968. — В. 1. — Т. 7. — С. 115—120.
- ↑ Lin M. S., Naphtali L. M. Prediction of vapor-liquid equilibria with the Benedict — Webb — Rubin equation of state // The American Institute of Chemical Engineers Journal. — 1963. — В. 5. — Т. 9. — С. 580—584.
- ↑ Orye R. V. Prediction and Correlation of Phase Equilibria and Thermal Properties with the BWR Equation of State // Industrial & Engineering Chemistry Process Design and Development. — 1969. — В. 4. — Т. 8. — С. 579—588.
- ↑ Starling К. E. // Hydrocarbon Processing. — 1971. — В. 3. — Т. 50. — С. 101.
- ↑ Starling К. E. Fluid Thermodynamic Properties for Light Petroleum Systems. — Gulf Publishing Company, 1973.
- ↑ Edmister W. C., Vairogs J., Klekers A. J. A generalized B—W—R equation of state // The American Institute of Chemical Engineers Journal. — 1968. — В. 3. — Т. 14. — С. 479.
- ↑ Opfell J. B., Sage B. H., Pitzer K. S. Application of Benedict Equation to Theorem of Corresponding States // Industrial and Engineering Chemistry. — 1956. — В. 11. — Т. 48. — С. 2069—2076.
- ↑ Lee B. I., Kesler M. G. A generalized thermodynamic correlation based on three-parameter corresponding states // The American Institute of Chemical Engineers Journal. — 1975. — В. 3. — Т. 21. — С. 510—527.
- ↑ Pitzer К. S., Curl R. F. et al Volumetric and Thermodynamic Properties of Fluids—Enthalpy, Free Energy, and Entropy // Industrial and Engineering Chemistry. — 1958. — Т. 50. — С. 265—274.
- ↑ Hopke S. W. Application of equations of state in Exxon's production operations // ACS Symposium Series. — 1977. — Т. 60. — С. 221—223.
- ↑ Nishiumi H. Thermodynamic property prediction of C10 to C20 paraffins and their mixtures by the generalized BWR equation of state // Journal of Chemical Engineering of Japan. — 1980. — В. 1. — Т. 13. — С. 74—76.
- ↑ Nishiumi H. An improved generalized BWR equation of state with three polar parameters applicable to polar substances. // Journal of Chemical Engineering of Japan. — 1980. — В. 3. — Т. 13. — С. 178—183.
Wikimedia Foundation. 2010.
Уравнение состояния Бенедикта — Уравнение состояния Стат … Википедия
Уравнение состояния Редлиха — Квонга — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа … Википедия
Уравнение состояния Редлиха — Уравнение состояния Стат … Википедия
Уравнение состояния Барнера — Адлера — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа … Википедия
Уравнение состояния Ли — Эрбара — Эдмистера — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа … Википедия
Уравнение состояния Суги — Лю — Уравнение состояния Статья является частью серии «Термодинамика». Уравнение состояния идеального газа Уравнен … Википедия
Уравнение состояния Барнера — Уравнение состояния Стат … Википедия
Уравнение состояния Ли — Уравнение состояния Стат … Википедия
Уравнение состояния Суги — Уравнение состояния Статья является час … Википедия
Уравнение состояния идеального газа — Уравнение состояния Стат … Википедия

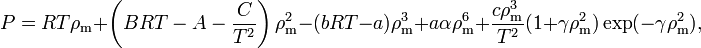
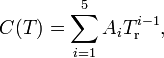
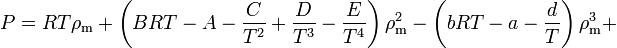
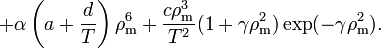
![\frac{P_\mathrm{r}V^{(0)}_\mathrm{r}}{T_\mathrm{r}}=1+\frac{B}{V^{(0)}_\mathrm{r}}+\frac{C}{\left(V^{(0)}_\mathrm{r}\right)^2}+\frac{D}{\left(V^{(0)}_\mathrm{r}\right)^5}+\frac{c_4}{T^3_\mathrm{r}\left(V^{(0)}_\mathrm{r}\right)^2}\left[\beta+\frac{\gamma}{\left(V^{(0)}_\mathrm{r}\right)^2}\right]\exp\left[-\frac{\gamma}{\left(V^{(0)}_\mathrm{r}\right)^2}\right],\qquad(*)](http://dic.academic.ru/pictures/wiki/files/101/ee5d217e473a9b39612cd025b8e70a73.png)