- Хлорид титана(IV)
-
Хлорид титана(IV) 
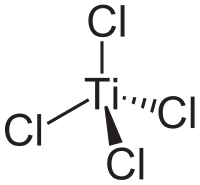
Общие Химическая формула TiCl4 Физические свойства Состояние (ст. усл.) бесцветная дымящая жидкость Молярная масса 189.71 г/моль Плотность 1.726 г/см³ Термические свойства Температура плавления -24.8 °C Температура кипения 136,4[1] °C Температура вспышки негорюч °C Энтальпия образования (ст. усл.) -804,16 кДж/моль Химические свойства Растворимость в воде реагирует с водой, образуя TiO2 и HCl г/100 мл Растворимость в растворим в этаноле г/100 мл Структура Кристаллическая структура тетраэдрическая Дипольный момент 0 Д Классификация Рег. номер CAS 7550-45-0 Номер ООН 1838 Регистрационный номер EC 231-441-9 RTECS XR1925000 Безопасность Токсичность Хлорид титана(IV) (тетрахлорид титана, титан четыреххлористый, тетрахлортитан) — бесцветная подвижная прозрачная жидкость, дымящая на воздухе. Химическая формула — TiCl4.
Содержание
Физические свойства
- Температура кипения: 136,4 °C[1]
- Температура плавления: −24,1 °C
- Относительная плотность (вода = 1): 1,7
- Растворимость в воде — растворяется
- Давление паров, кПа при 21,3 °C: 1,3
- Относительная плотность пара (воздух = 1): 6,5
Химические свойства
Гидролизуется в воде. Способен присоединять NH3, ароматические соединения, эфиры. Выше 500—600 °C окисляется О2 воздуха до ТiO2, в присутствии паров воды образуются также оксихлориды TiOCl2, Ti2O3Cl2. Бурно реагирует с водой с получением ТiO2·nН2О, в качестве промежуточных продуктов образуются гидрат TiCl4·5H2O и гидроксохлориды Ti(OH)nCl4-n·xH2O. Растворим в этаноле и диэтиловом эфире. С парами воды при 300—400 °C даёт ТiO2. Восстанавливается водородом Н2 и активными металлами до TiCl2 и TiCl3, затем до Ti. В TiCl4 растворим хлор Сl2 (7,6 % по массе при 20 °C), незначительно растворим хлороводород НСl. Смешивается во всех соотношениях с жидким НСl, а также с хлоридами Sn, С, Si. Растворим в соляной кислоте при пропускании газообразного НСl с получением ярко-жёлтого раствора править] Получение
При очень медленном добавлении воды с тщательным перемешиванием и охлаждением можно получить устойчивые концентрированные растворы TiCl4. Для получения TiCl4 высокой чистоты используют ректификацию и адсорбцию примесей на силикагеле. Очищают тетрахлорид титана фильтрованием, гидролизом с помощью увлажнённого NaCl (удаление As), восстановлением медью, алюминием или сероводородом H2S (удаление ванадия, серы, хрома, органических соединений), дистилляцией и ректификацией.
Также тетрахлорид титана можно получить, проделав следующие реакции:
Хлорид титана(IV) производится в процессе хлорирования, который предусматривает обработку руды титана. Как правило, реакция ильменита (FeTiO3) с углеродом происходит под хлором при температуре 900 °C. Примеси удаляются путём дистилляции:
Применение
Используют TiCl4 для получения титана, оксида TiO2, катализаторов (где происходит полимеризация этилена и пропилена, алкилирование ароматических углеводородов и др.) и как дымообразователь. Тетрахлорид титана применяется:
- в производстве губчатого титана, пигментной двуокиси титана;
- в качестве катализатора в химической промышленности (см. Катализаторы Циглера — Натта).
Примечания
- ↑ 1 2 Rocket NXT
Литература
- Зефиров Н.С. и др. т.4 Пол-Три // Химическая энциклопедия. — М.: Большая Российская Энциклопедия, 1995. — 639 с. — 20 000 экз. — ISBN 5-85270-092-4
Категории:- Соединения титана
- Хлориды
- Неорганические вещества
- Галогениды металлов
Wikimedia Foundation. 2010.



